Анестезія при черепно-мозковій травмі: зниження ризику ускладнень
Аналізуємо, як досягти нейропротекції та водночас забезпечити достатню аналгезію і седацію в пацієнтів із черепно-мозковою травмою
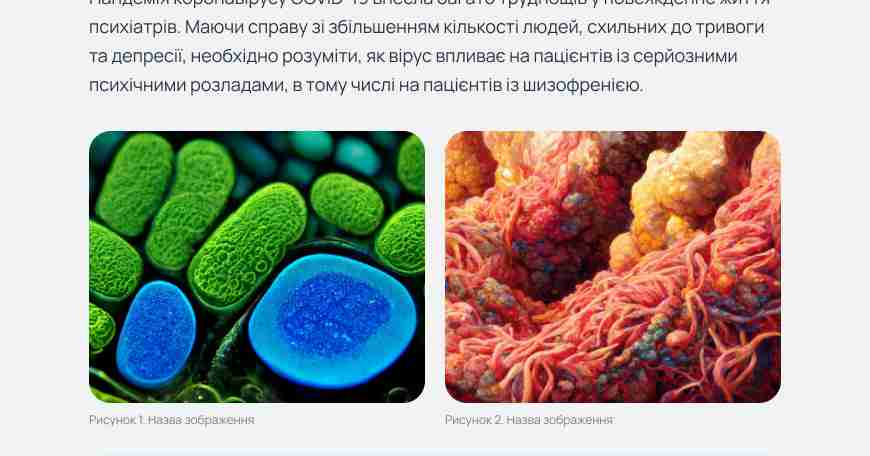
Анестезія при черепно-мозковій травмі: зниження ризику ускладнень
Хірургічні втручання та анестезія в пацієнтів із черепно-мозковою травмою (ЧМТ) можуть спричиняти вторинні ушкодження головного мозку. Основними факторами, що погіршують результати лікування, є гіпотензія, гіпоксемія, порушення газообміну, дисглікемія, лихоманка і підвищений внутрішньочерепний тиск1.
Ключовими завданнями є не лише забезпечення достатньої аналгезії та седації під час операції, але й активне запобігання вторинним ушкодженням і досягнення нейропротекції1.
Інтраопераційні цілі: як мінімізувати вторинне ушкодження мозку
Для запобігання вторинним ушкодженням мозку під час анестезії в пацієнтів із ЧМТ важливо підтримувати оптимальний церебральний перфузійний тиск (ЦПТ) і контрольований внутрішньочерепний тиск (ВЧТ). Цього досягають завдяки гемодинамічній підтримці та вентиляції легень1.
Гемодинамічна підтримка
Основна мета інтраопераційного гемодинамічного менеджменту — забезпечення достатнього мозкового кровотоку, для досягнення якого, за рекомендаціями Фонду досліджень черепно-мозкової травми (BTF), необхідно дотримуватися таких ключових показників2:
- Середній артеріальний тиск (САТ) ≥100 мм рт.ст. для пацієнтів віком від 50 до 69 років
- САТ ≥110 мм рт.ст. для пацієнтів віком від 15 до 49 або старше 70 років
- ВЧТ ≤22 мм рт.ст.
- ЦПТ у межах 60−70 мм рт.ст.
Формула розрахування ЦПТ1: ЦПТ = САТ – ВЧТ
Важливо, що зусилля з оптимізації ЦПТ насамперед має бути спрямовано на контроль підвищеного ВЧТ, а не на збільшення САТ за допомогою вазопресорів1.
Раптове підвищення САТ може призвести до вторинних ускладнень, як-от крововилив, набряк мозку чи підвищення ВЧТ, через збільшення об'єму мозкової крові1.
Різке ж зниження САТ пов'язано з гіпоперфузією та ішемією. Інтраопераційна гіпотензія може виникнути після видалення кісткового клаптя та розтину твердої мозкової оболонки. Тривалість такої гіпотензії обернено корелює з неврологічними прогнозами1.
У разі потреби у вазопресорах найчастіше застосовують фенілефрин, який має доведену ефективність. Для підтримання еуволемії рекомендовано використовувати теплий неглюкозовмісний ізотонічний кристалоїд1.
Параметри вентиляції легень
Цілі оксигенації та вентиляції для пацієнтів із ЧМТ1:
- Парціальний тиск кисню (PaO2) — 60–200 мм рт.ст.
- Насичення крові киснем (SpO2) — >90%
- Парціальний тиск вуглекислого газу (PCO2) — 35–38 мм рт.ст., якщо не потрібна терапевтична гіпервентиляція
Гіпервентиляцію слід застосовувати вибірково. Рутинна гіпервентиляція не рекомендована для пацієнтів із помірною або важкою ЧМТ протягом перших 24–48 годин1.
Однак у деяких випадках гіпервентиляція може бути необхідною для зниження ВЧТ або зменшення набряку мозку. У таких ситуаціях є допустимою легка або помірна гіпервентиляція з PaCO2 28–35 мм рт.ст. як тимчасове втручання для контролю кризів підвищеного ВЧТ.
Слід уникати PaCO2 ≤25 мм рт.ст., адже звуження судин через гіпервентиляцію може призвести до ішемії в тканинах мозку, які віднесено до групи ризику вторинних ушкоджень після ЧМТ1,2.
Оцінювання вентиляції має базуватися на аналізі газів крові, а не на концентрації вуглекислого газу в кінці видиху (EtCO2). Хоч EtCO2 добре корелює з PCO2, деякі фактори, такі як вік, захворювання легень або хірургічне позиціонування, можуть зумовити значні розбіжності між цими показниками1.
Вибір лікарських засобів для анестезії
Пацієнти з підозрою на внутрішньочерепну гіпертензією не потребують премедикації1.
Для індукування анестезії рекомендовано застосовувати техніку швидкої послідовної індукції та інтубації, з застосуванням таких ЛЗ1:
- Фентаніл 2–4 мкг/кг в/в
- Лідокаїн 1–1,5 мг/кг в/в
- Пропофол 1,5–2 мг/кг в/в
- Дитилін 1–2,5 мг/кг
Пацієнтам із імовірною внутрішньочерепною гіпертензією слід додатково вводити дефасцикулювальну дозу рокуронію 2 мг в/в і дитилін 1,5–2 мг/кг.
Якщо травму шийного відділу хребта не виключено, слід мінімізувати рухи шийного відділу під час маніпуляцій із дихальними шляхами1
Підтримання анестезії1
Севофлуран <1 МАК або пропофол 70–140 мкг/кг/хв, титрований відповідно до показників обробленої ЕЕГ
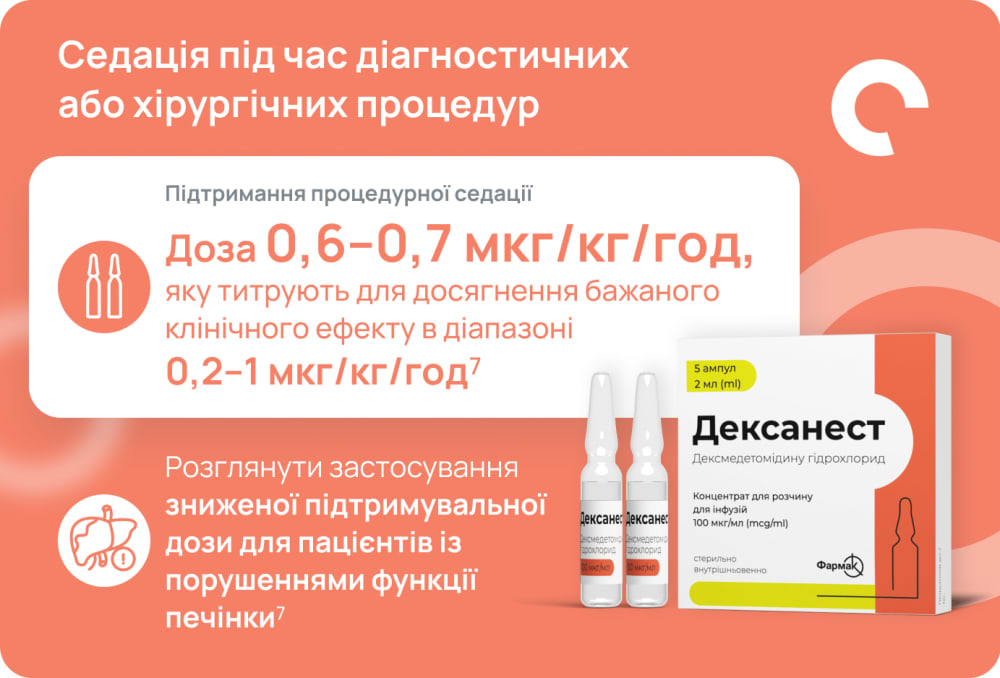
Низькі дози кетаміну (до 10 мг/год) або дексмедетомідину (0,2–0,6 мкг/кг/год) як допоміжні засоби
Фентаніл 1–2 мкг/кг кожні 1–2 години залежно від гемодинамічного статусу
Міорелаксант, титрований відповідно до показників нервово-м'язової провідності, виміряних за допомогою TOF
Ондансетрон 4 мг в/в за годину до пробудження
Контроль болю1
Морфін 3–5 мг в/в за 30 хвилин до пробудження як альтернативний метод знеболення
Парацетамол 1000 мг в/в для посилення аналгезії



Основні тези
Для запобігання вторинним ушкодженням мозку під час анестезії в пацієнтів із ЧМТ необхідно підтримувати церебральний перфузійний тиск (ЦПТ) на рівні 60–70 мм рт.ст. і внутрішньочерепний тиск (ВЧТ) ≤22 мм рт.ст.2
Інтраопераційна мета для середнього артеріального тиску (САТ): ≥100 мм рт.ст. для пацієнтів віком 50–69 років і ≥110 мм рт.ст. для пацієнтів віком 15–49 або старше 70 років2
Формула розрахування ЦПТ: ЦПТ = САТ – ВЧТ1
Зусилля з оптимізації ЦПТ насамперед має бути спрямовано на контроль підвищеного ВЧТ, а не на збільшення САТ за допомогою вазопресорів1
Рутинну гіпервентиляцію не рекомендовано для пацієнтів із помірною або важкою ЧМТ протягом перших 24–48 годин1
Є допустимою легка або помірна гіпервентиляція з PaCO2 28–35 мм рт.ст. як тимчасове втручання для контролю кризів підвищеного ВЧТ1
Для індукування анестезії слід використовувати техніку швидкої послідовної індукції та інтубації1
Для підтримання анестезії застосовують севофлуран або пропофол, низькі дози кетаміну або дексмедетомідину як допоміжні засоби, фентаніл, міорелаксант, титрований за показниками TOF, та ондансетрон1
Дексмедетомідин запобігає та лікує пароксизмальну симпатичну гіперактивність, зменшує тривалість перебування на штучній вентиляції та госпіталізації, знижує смертність у пацієнтів із ЧМТ5,6
BTF (Brain Trauma Foundation) — Фонд досліджень черепно-мозкової травми
ETCO2 — рівень вуглекислого газу в повітрі, що видихається
PaO2 — парціальний тиск кисню
PCO2— парціальний тиск вуглекислого газу
SpO2 — насичення крові киснем
TOF (train-of-for) — один із видів моніторування нервово-мʼязової провідності
в/в — внутрішньовенно
ВЧТ — внутрішньочерепний тиск
ЕЕГ — електроенцефалографія
МАК — мінімальна альвеолярна концентрація
САТ — середній артеріальний тиск
ЦПТ — церебральний перфузійний тиск
ЧМТ — черепно-мозкова травма
- Anesthesia for patients with acute traumatic brain injury. Available at: https://www.uptodate.com/contents/anesthesia-for-patients-with-acute-traumatic-brain-injury?search=anesthesia%20for%20tbi&source=search_result&selectedTitle=1%7E150&usage_type=default&display_rank=1#H2505316255 (Last access: 20.09.2024).
- Carney N., Totten A.M., O'Reilly C. et al. Guidelines for the Management of Severe Traumatic Brain Injury, Fourth Edition. Neurosurgery. 2017; 80(1):6−15. DOI: 10.1227/NEU.0000000000001432
- Hu Y., Zhou H., Zhang H. et al. The neuroprotective effect of dexmedetomidine and its mechanism. Front Pharmacol. 2022; 13:965661. DOI: 10.3389/fphar.2022.965661
- Hatfield J., Soto A.L., Kelly-Hedrick M. et al. Safety, Efficacy, and Clinical Outcomes of Dexmedetomidine for Sedation in Traumatic Brain Injury: A Scoping Review. J Neurosurg Anesthesiol. 2024; 36(2):101−108. DOI: 10.1097/ANA.0000000000000907
- Jerousek C.R., Reinert J.P. The Role of Dexmedetomidine in Paroxysmal Sympathetic Hyperactivity: A Systematic Review. Ann Pharmacother. 2024; 58(6):614−621. DOI: 10.1177/10600280231194708
- Liu S.Y., Kelly-Hedrick M., Komisarow J. et al. Association of Early Dexmedetomidine Utilization With Clinical Outcomes After Moderate-Severe Traumatic Brain Injury: A Retrospective Cohort Study. Anesth Analg. 2024; 139(2):366−374. DOI: 10.1213/ANE.0000000000006869
- Інструкція для медичного застосування лікарського засобу Дексанест®. РП №UA/20014/01/01.








