Нез’ясоване безпліддя: коли стандартна спермограма не пояснює проблеми
Нормальні параметри спермограми не гарантують фертильності. Дізнайтесь, яку роль у цьому відіграє оксидативний стрес та як вести таких пацієнтів.
Нез’ясоване безпліддя: коли стандартна спермограма не пояснює проблеми
Ненастання вагітності впродовж року — типова скарга пацієнтів на прийомі в лікаря. Під час подальшого обстеження виявляється, що в жінки немає очевидних порушень репродуктивного здоров’я, а результати спермограми партнера відповідають нормі. В таких випадках виникає запитання: що може стояти за незрозумілим безпліддям? Чоловічі порушення фертильності є причиною майже половини всіх випадків безпліддя в парах1. Зазвичай вони пов’язані зі зменшенням кількості або розладами функції сперматозоїдів1.
Згідно з рекомендаціями ВООЗ діагностика чоловічого безпліддя зазвичай ґрунтується на стандартному аналізі параметрів сперми2. Водночас приблизно в 25% випадків показники спермограми залишаються в межах норми1.
Одним із нових і актуальних механізмів, який розглядають у патогенезі чоловічого безпліддя, є оксидативний стрес2.
Оксидативний стрес визначається як дисбаланс між утворенням активних форм кисню (АФК) і захисною дією антиоксидантних систем, відповідальних за їх нейтралізацію та видалення3. Фізіологічні рівні АФК важливі для таких процесів, як сперматогенез, дозрівання сперматозоїдів, капацитація, гіперактивація, хемотаксис, акросомна реакція та злиття сперматозоїдів з ооцитами4.
Роль оксидативного стресу в патогенезі чоловічого безпліддя
Надмірне продукування АФК призводить до пошкодження сперматозоїдів4. Їм бракує необхідних систем репарації, і вони не можуть відновити оксидативні ушкодження3. До того ж мембрани сперматозоїдів багаті на поліненасичені жирні кислоти, що робить їх особливо сприйнятливими до перекисного окиснення ліпідів3.
Оксидативний стрес спричиняє ураження аксонем, зниження життєздатності сперматозоїдів, збільшення морфологічних дефектів середньої частини сперматозоїдів3. Він призводить до втрати цілісності мембрани і структурного пошкодження ДНК3.
Це зумовлює3:
Зниження рухливості сперматозоїдів
Апоптоз сперматозоїдів
Порушення взаємодії між сперматозоїдами та яйцеклітинами3.
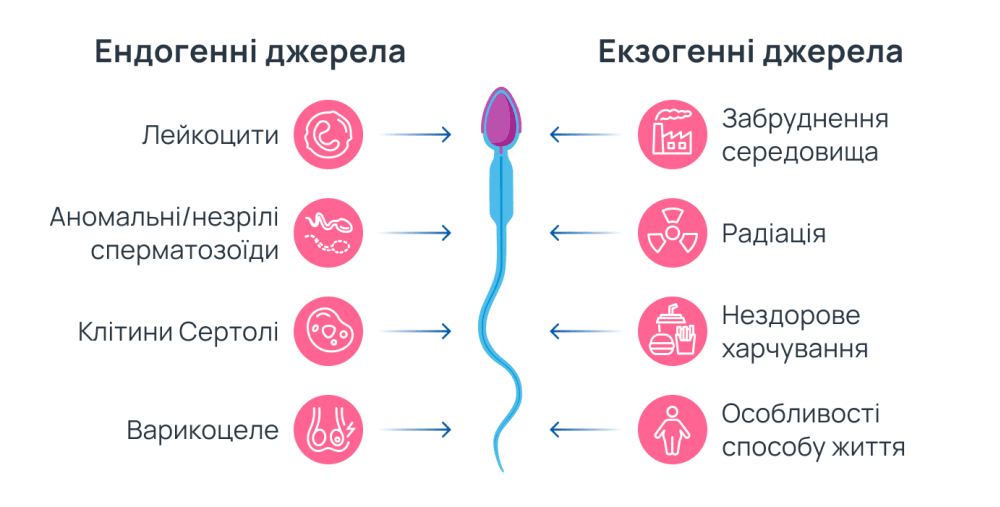
На порушення окисно-відновного балансу можуть впливати як екзогенні, так і ендогенні джерела АФК4.
Навіть за нормальних показників спермограми — таких як концентрація, рухливість і морфологія сперматозоїдів — не завжди вдається виявити приховані функціональні порушення1. Зокрема, стандартний аналіз еякуляту не дає змоги оцінити рівень оксидативного стресу2.
Лабораторне оцінювання оксидативного стресу
Ідентифікація маркерів оксидативного стресу дає змогу зрозуміти патофізіологію захворювання, прогноз і реакцію на лікування4. Є різні методи для оцінювання окисно-відновного балансу та АФК, серед яких4:
Метод хемілюмінесценції
Оцінювання загальної антиоксидантної здатності
Окисно-відновний потенціал еякуляту
Тест на відновлення нітросинього тетразолію
Тест на відновлення цитохрому С
Вимірювання внутрішньоклітинних активних форм кисню на основі проточної цитометрії
Сучасні методи дають змогу точніше виявляти ознаки оксидативного стресу в еякуляті4. Однак в Україні тест на окисно-відновний потенціал еякуляту на сьогодні недоступний у більшості клінічних лабораторій*. Тому варто орієнтуватися на непрямі ознаки оксидативного стресу, клінічний контекст і анамнез пацієнта.
Методи зниження оксидативного стресу
У клінічній практиці все ще бракує стандартизованих підходів до лікування пацієнтів з ідіопатичним або пов’язаним із цим фактором чоловічим безпліддям4. У зв’язку з цим застосовують різні терапевтичні стратегії, спрямовані на покращення якості сперми та зменшення рівня оксидативного стресу4.
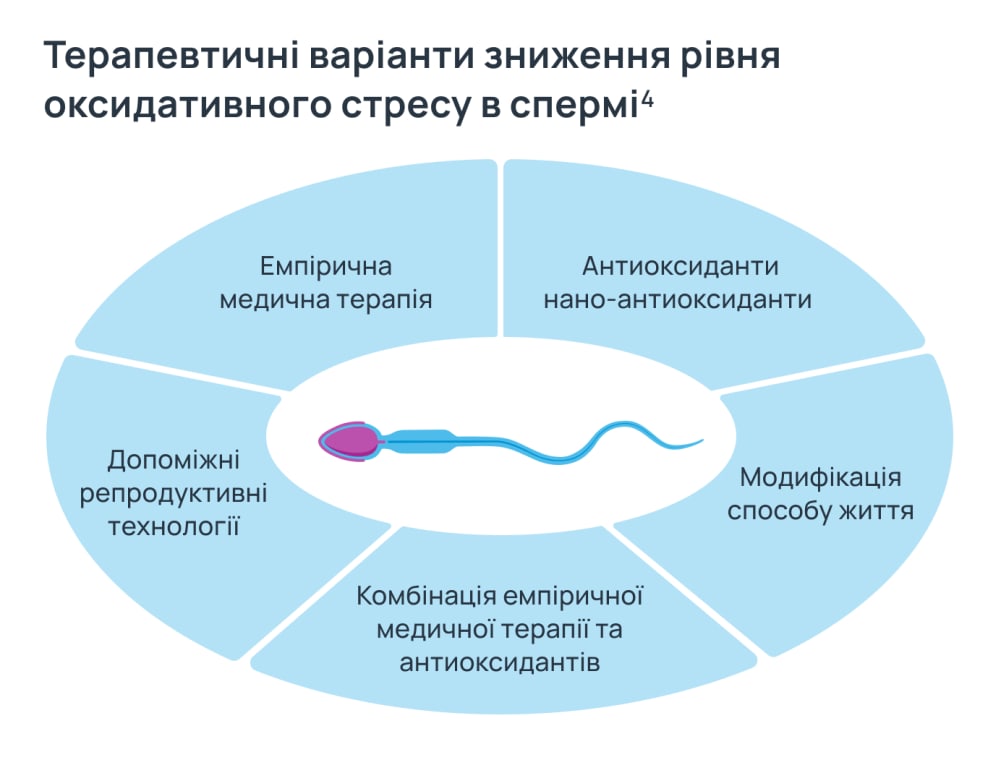
Дослідники припускають, що застосування антиоксидантів може захищати сперматозоїди від АФК, які утворюються аномальними сперматозоїдами5. Також антиоксиданти можуть нейтралізувати АФК, що продукуються лейкоцитами, і запобігають фрагментації ДНК5. Антиоксиданти можуть покращувати якість еякуляту в курців і знижувати ступінь кріопошкодження сперматозоїдів5.
Серед інших ефектів антиоксидантів припускають блокування передчасного дозрівання сперматозоїдів, підвищення їхньої активності та можливе покращення результатів застосування допоміжних репродуктивних технологій5. Наразі відсутні остаточні докази впливу антиоксидантів на якість сперми і немає зареєстрованих лікарських засобів за цим показанням.
Для покращення чоловічої фертильності може бути використаний доведений антиоксидантний вплив таких речовин5,6,7:
Вітаміни А, Е і С
Коензим Q10
Фолієва кислота
Ресвератрол
Марганець
Інозитоли
Особливу увагу приділяють марганцю та інозитолам, оскільки вони відіграють важливу роль у підтриманні процесів сперматогенезу і покращенні якості сперматозоїдів завдяки поліпшенню окисно-відновного балансу6,8.
Найпоширенішими формами інозитолів, які використовують у клінічній практиці, є міо-інозитол (МІ) та D-хіро-інозитол (DCI)6. Фактично кожен орган або тканина має певне співвідношення MI:DCI, що є фундаментальним для їхнього нормального функціонування6. Міо-інозитол впливає на покращення здатності сперматозоїдів до запліднення та їхньої рухливості6. Він є вторинним месенджером гонадотропіну фолікулостимулювального гормону (ФСГ)6. На рівні яєчок ФСГ відіграє ключову роль у контролі кількості та функції клітин Сертолі, сприяючи диференціації цих клітин, він необхідній для підтримання нормального сперматогенезу6.
Марганець забезпечує захист організму від АФК8. Цей мікроелемент покращує рухливість сперматозоїдів та їхню життєздатність, мінімізуючи оксидативний стрес8. Дефіцит марганцю має негативний вплив на об'єм сперми та нормальну морфологію сперматозоїдів8.
Окрім позитивного впливу на чоловічу репродуктивну систему, нутритивна підтримка з інозитолами і марганцем, згідно з припущенням дослідників, може захищати також яйцеклітини від оксидативного стресу та покращувати їхню якість9.
Основні тези
Згідно з рекомендаціями ВООЗ діагностика чоловічого безпліддя зазвичай ґрунтується на стандартному аналізі параметрів сперми2. Водночас приблизно в 25% випадків чоловічого безпліддя показники спермограми залишаються в межах норми1
Одним із нових і актуальних механізмів, який розглядають у патогенезі чоловічого безпліддя, є оксидативний стрес2
Сперматозоїдам бракує необхідних систем репарації, і вони не можуть відновити оксидативні пошкодження3. До того ж мембрани сперматозоїдів багаті на поліненасичені жирні кислоти, що робить їх особливо сприйнятливими до перекисного окиснення ліпідів3
Стандартний аналіз еякуляту не дає змоги оцінити рівень оксидативного стресу1
Дослідження показали, що застосування антиоксидантів захищає сперматозоїди від АФК5
Міо-інозитол впливає на покращення здатності сперматозоїдів до запліднення та їхньої рухливості6
Марганець забезпечує захист організму від АФК8. Цей мікроелемент покращує рухливість сперматозоїдів та їхню життєздатність, мінімізуючи оксидативний стрес8
*За результатами відкритого пошуку (станом на травень 2025 року), цей тест на сьогодні недоступний у більшості лабораторій в Україні.
DCI — D-хіро-інозитол
АФК — активні форми кисню
ВООЗ — Всесвітня організація охорони здоров’я
ДНК — дезоксирибонуклеїнова кислота
МІ — міо-інозитол
ФСГ — фолікулостимулювальний гормон
- Palani A., Alahmar A. Impact of oxidative stress on semen parameters in normozoospermic infertile men: a case-control study. Afr J Urol. 2020; 26(50). DOI: https://doi.org/10.1186/s12301-020-00061-6
- Mannucci A., Argento F.R., Fini E. et al. The Impact of Oxidative Stress in Male Infertility. Front Mol Biosci. 2022; 8:799294. DOI: 10.3389/fmolb.2021.799294
- Kurkowska W., Bogacz A., Janiszewska M. et al. Oxidative Stress is Associated with Reduced Sperm Motility in Normal Semen. Am J Mens Health. 2020; 14(5):1557988320939731. DOI: 10.1177/1557988320939731
- Pavuluri H., Bakhtiary Z., Panner S.M.K. et al. Oxidative Stress-Associated Male Infertility: Current Diagnostic and Therapeutic Approaches. Medicina (Kaunas). 2024; 60(6):1008. DOI: 10.3390/medicina60061008
- Agarwal A., Makker K., Sharma R. Clinical relevance of oxidative stress in male factor infertility: an update. Am J Reprod Immunol. 2008; 59(1):2–11. DOI: 10.1111/j.1600-0897.2007.00559.x
- De Luca M.N., Colone M., Gambioli R. et al. Oxidative Stress and Male Fertility: Role of Antioxidants and Inositols. Antioxidants (Basel). 2021; 10(8):1283. DOI: 10.3390/antiox10081283
- Dimitriadis F., Borgmann H., Struck J.P. et al. Antioxidant Supplementation on Male Fertility — A Systematic Review. Antioxidants. 2023; 12(4):836. DOI: https://doi.org/10.3390/antiox12040836
- Chao H.-H., Zhang Y., Dong P-Y. et al. Comprehensive review on the positive and negative eects of various important regulators on male spermatogenesis and fertility. Front. Nutr. 2023; 9:1063510. DOI: 10.3389/fnut.2022.106351
- Інструкція з використання. Дієтична добавка Фолатін, порошок для орального розчину.
Виробник: АТ «Фармак», 04080, м. Київ, вул. Кирилівська, 63, тел.: +38 (044) 496-87-87/e-mail: [email protected] /вебсайт: www.farmak.ua








