Вплив оксидативного стресу на оваріальний резерв
Після 35 років фертильність природно знижується, а оксидативний стрес прискорює цей процес. Дізнайтеся про роль нутрієнтів у збереженні якості ооцитів
Вплив оксидативного стресу на оваріальний резерв
У сучасному суспільстві з різних причин дедалі більше жінок відкладають народження дітей на пізніший вік. Водночас уже після 30 років спостерігається поступове зниження фертильності, яке набуває клінічного значення у віці 35–40 років. Однією з ключових причин цього є старіння яєчників, яке відіграє істотну роль у розвитку жіночого безпліддя. З віком зменшуються як кількість, так і якість фолікулів та яйцеклітин, що супроводжується поступовим виснаженням оваріального резерву1.
Серед ключових чинників, що спричиняють погіршення якості яйцеклітин із віком, є оксидативний стрес (ОС)1,2. Тому пошук методів, спрямованих на його зменшення, набуває особливої актуальності в межах стратегій, що дають змогу сповільнити оваріальне старіння та підтримати якість яйцеклітин.
Як оксидативний стрес впливає на репродуктивне здоров’я
Активні форми кисню (АФК) за фізіологічних умов беруть участь у низці ключових клітинних процесів2. Зокрема, у фолікулогенезі, дозріванні яйцеклітин, овуляції, заплідненні, імплантації ембріона та розвитку плода3. У нормі підтримується баланс між утворенням вільних радикалів і системою антиоксидантного захисту. Однак за надмірного утворення АФК цей баланс порушується, що призводить до розвитку ОС і пошкодження здорових клітин2.
ОС супроводжується процесами, які погіршують клітинні функції та негативно вливають на процеси старіння2:
Дисфункцією мітохондрій
Окисленням білків
Пероксидним ураженням ліпідів
Ушкодженням і мутаціями ДНК
Загальновизнано, що ОС має негативні наслідки для яєчників, матки, яйцеклітин та ембріонів2. У яєчниках ОС обмежує дозрівання фолікулів та яйцеклітин, що призводить до зменшення їх кількості та компетентності3. А також до аномального збільшення фолікулостимулювального гормону2.
Окислювальне пошкодження яйцеклітин спричиняє фрагментацію ДНК, мітохондріальну дисфункцію, анеуплоїдію та, відповідно, зниження рівня запліднення. Висока частота анеуплоїдії є основною причиною спонтанних абортів і зниження фертильності2
З віком вироблення АФК збільшується та зумовлює «старіння» яєчників. Кореляція між ОС і старінням яєчників пов'язана з порушеннями мітохондріальних функцій та мутаціями в яйцеклітинах, антиоксидантний захист яких із часом послаблюється2.
Відмінності в розвитку яйцеклітин і фолікулів між молодими та яєчниками середнього репродуктивного віку4
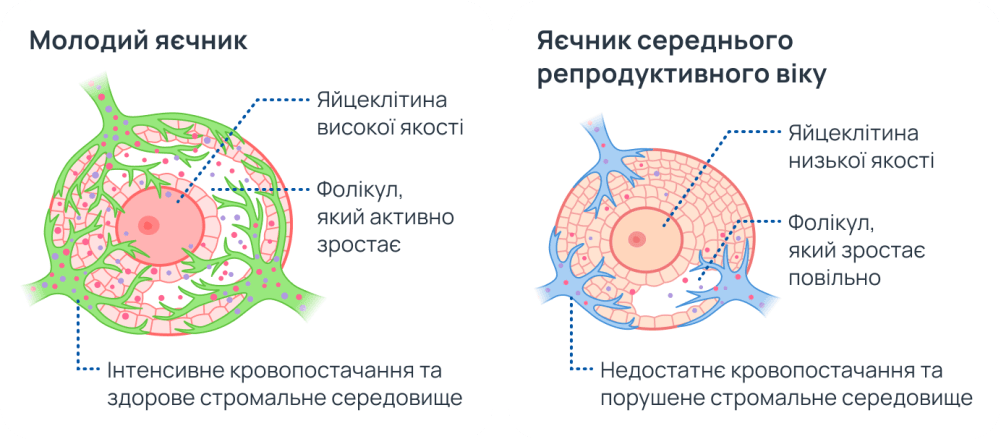
Навіть у разі успішного запліднення ОС може перешкоджати подальшому розвитку вагітності. Зокрема, у матці він ускладнює процес імплантації та асоціюється з деякими патологічними станами, такими як ендометріоз, прееклампсія та порушення плацентації2.
Усе це підвищує ризик затримання внутрішньоутробного розвитку плода й мимовільного переривання вагітності2. Тому антиоксидантна система є необхідною для нейтралізації АФК, захисту репродуктивних клітин і тканин, а також підтримання нормальної фертильності5.
Яка антиоксидантна підтримка показана пацієнткам для покращення фертильності
Для протидії надлишку АФК клітини мають комплексну систему антиоксидантного захисту. Вона включає як ферментативні антиоксиданти, такі як супероксиддисмутаза, каталаза і глутатіонпероксидаза, так і неферментативні антиоксиданти5.
Антиоксиданти поділяються за походженням на ендогенні — ферменти та малі молекули, що синтезуються в організмі, — і ті, що надходять з їжею. До харчових антиоксидантів належать фенольні сполуки, каротиноїди, вітаміни і мікроелементи. Тому вживання нутритивних добавок з антиоксидантним впливом може допомогти пом'якшити вплив окислювального пошкодження5.
Серед речовин з антиоксидантним потенціалом особливу увагу привертають мікроелементи й метаболічно активні сполуки, які беруть участь у регуляції репродуктивної функції5. Серед таких речовин марганець та інозитоли5,6.
Марганець
Марганець, особливо у формі іонів Mn2+, є важливим компонентом активних центрів багатьох ферментів. Він виконує роль кофактора для низки ферментів, зокрема марганцевої супероксиддисмутази, аргінази, глутамінсинтетази, фосфоенолпіруватдекарбоксилази та піруваткарбоксилази. Марганцева супероксиддисмутаза локалізується в мітохондріях і є основним захистом від оксидативного стресу. До того ж марганець опосередковано діє на окисно-відновний стан заліза, міді та інших перехідних металів, які також впливають на репродуктивний стан5.
Тож завдяки своїм антиоксидантним властивостям марганець може відігравати захисну роль у жіночому репродуктивному здоров'ї та підвищувати жіночу фертильність7.
Інозитоли
Інозитоли привертають увагу завдяки потенційним перевагам у репродуктивній терапії, своїй ключовій ролі в клітинній сигналізації та антиоксидантному впливі. Найпоширенішими ізомерними формами інозитолу є міо-інозитол та Д-хіро-інозитол6.
Основні функції інозитолів пов’язані з сигнальними шляхами інсуліну, гонадотропінів, а також процесами перебудови цитоскелету. Тож інозитоли виступають медіаторами важливих фізіологічних процесів, таких як енергетичний метаболізм, клітинна рухливість, а в яєчниках — розвиток фолікулів протягом менструального циклу6.
Інозитоли можуть впливати на дозрівання яйцеклітин, що робить їх потенційними засобами для відновлення овуляції. Інозитоли збільшують рівень ферментних антиоксидантів — супероксиддисмутази, каталази та глутатіону, а також покращують морфологію зростання клітин і синтез ліпідів у клітинних мембранах6.
Збалансовані інозитолами метаболічні процеси та оптимальний рівень глюкози є критично важливими для дозрівання фолікулів і покращення жіночої фертильності. Вони також забезпечують належну клітинну рухливість, необхідну під час ембріогенезу (зокрема, для закриття нервової трубки), і сприяють фізіологічному перебігу вагітності6.
Тому добавки з інозитолами та марганцем можна розглядати як перспективну стратегію для покращення якості ооцитів, ембріонів та, як наслідок, перебігу вагітності в жінок віком від 35 років
Основні тези
Після 30 років спостерігають поступове зниження фертильності, яке набуває клінічного значення у віці 35–40 років1
Серед ключових чинників, що спричиняють погіршення якості яйцеклітин із віком, є оксидативний стрес1,2
Антиоксидантна система є необхідною для нейтралізації АФК, захисту репродуктивних клітин і тканин, а також підтримання нормальної фертильності5
Використання нутритивних добавок з антиоксидантною дією може допомогти пом'якшити вплив окислювального пошкодження5
АФК — активні форми кисню
ДНК — дезоксирибонуклеїнова кислота
ОС — оксидативний стрес
- Bao S., Yin T., Liu S. Ovarian aging: energy metabolism of oocytes. J Ovarian Res. 2024; 17(118). DOI: https://doi.org/10.1186/s13048-024-01427-y
- Ra K., Park S.C., Lee B.C. Female Reproductive Aging and Oxidative Stress: Mesenchymal Stem Cell Conditioned Medium as a Promising Antioxidant. International Journal of Molecular Sciences. 2023; 24(5):5053. DOI: https://doi.org/10.3390/ijms24055053
- Chen Y., Yang J., Zhang L. The Impact of Follicular Fluid Oxidative Stress Levels on the Outcomes of Assisted Reproductive Therapy. Antioxidants (Basel). 2023; 12(12):2117. DOI: 10.3390/antiox12122117
- Wang G., Yang R., Zhang H. Ovarian vascular aging: a hidden driver of mid-age female fertility decline. npj Aging. 2025; 11(24). DOI: https://doi.org/10.1038/s41514-025-00216-1
- Wróblewski M., Wróblewska W., Sobiesiak M. The Role of Selected Elements in Oxidative Stress Protection: Key to Healthy Fertility and Reproduction. International Journal of Molecular Sciences. 2024; 25(17):9409. DOI: https://doi.org/10.3390/ijms25179409
- Placidi M., Casoli G., Tatone C. et al. Myo-Inositol and Its Derivatives: Their Roles in the Challenges of Infertility. Biology. 2024; 13(11):936. DOI: https://doi.org/10.3390/biology13110936
- Kapper C., Oppelt P., Ganhör C. et al. Minerals and the Menstrual Cycle: Impacts on Ovulation and Endometrial Health. Nutrients. 2024; 16(7):1008. DOI: 10.3390/nu16071008








